【行业】医药-关注疫情防控与业绩成长双主线(19页)
3 月 15 日,国家药监局召开党组(扩大)会议,传达学习习总书记在全国两会期间的重要讲话精神和全国两会精神,研究部署贯彻落实措施。会议要求持续做好新冠病毒疫苗的保质量、保供应工作,加快推动新冠病毒治疗药物、新冠病毒抗原检测试剂个人自测产品审批上市,强化防疫产品的质量监管,扎实做好内部防控工作,全力服务保障疫情防控大局。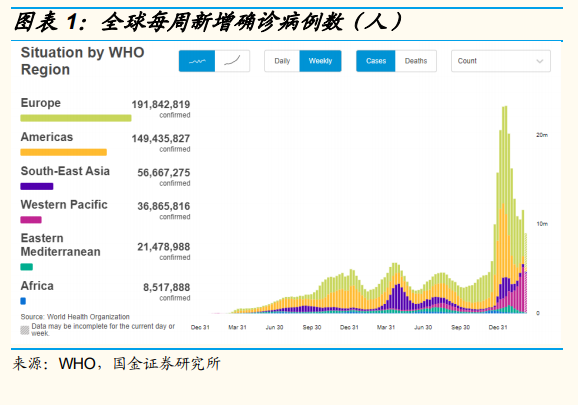 3 月 15 日,国家卫健委发布《新型冠状病毒肺炎诊疗方案(试行第九版)》,新版诊疗方案针对德尔塔、奥密克戎等变异毒株传播特点和病理特征进行了修订。重点修订内容包括:①优化病例发现和报告程序。在核酸检测基础上,增加抗原检测作为补充,进一步提高病例早发现能力,同时提高疑似病例诊断或排除效率;②对病例实施分类收治,从之前的疑似及确诊病例全部在定点医院治疗,修改为轻型病例实行集中隔离管理、普通型/重型/危重型病例和有重型高危因素的病例应在定点医院集中治疗;③将国家药监局批准的两种特异性抗新冠病毒药物写入诊疗方案,即辉瑞新冠口服药Paxlovid(PF-07321332/利托那韦片)和腾盛博药中和抗体(安巴韦单抗/罗米司韦单抗注射液);④中医治疗内容进行了修订完善;⑤调整解除隔离管理、出院标准以及缩短了解除隔离管理、出院后监测时间。我们认为,新冠诊疗方案的调整一方面反映出我国在新冠检测、新冠特效药研发及批准、中医中药等特色医疗的应用等方面的阶段性成果,另一方面也适应了变异株带来的疫情特征的变化。
3 月 15 日,国家卫健委发布《新型冠状病毒肺炎诊疗方案(试行第九版)》,新版诊疗方案针对德尔塔、奥密克戎等变异毒株传播特点和病理特征进行了修订。重点修订内容包括:①优化病例发现和报告程序。在核酸检测基础上,增加抗原检测作为补充,进一步提高病例早发现能力,同时提高疑似病例诊断或排除效率;②对病例实施分类收治,从之前的疑似及确诊病例全部在定点医院治疗,修改为轻型病例实行集中隔离管理、普通型/重型/危重型病例和有重型高危因素的病例应在定点医院集中治疗;③将国家药监局批准的两种特异性抗新冠病毒药物写入诊疗方案,即辉瑞新冠口服药Paxlovid(PF-07321332/利托那韦片)和腾盛博药中和抗体(安巴韦单抗/罗米司韦单抗注射液);④中医治疗内容进行了修订完善;⑤调整解除隔离管理、出院标准以及缩短了解除隔离管理、出院后监测时间。我们认为,新冠诊疗方案的调整一方面反映出我国在新冠检测、新冠特效药研发及批准、中医中药等特色医疗的应用等方面的阶段性成果,另一方面也适应了变异株带来的疫情特征的变化。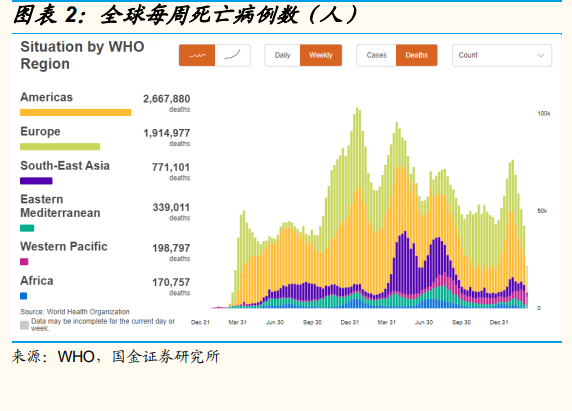 2022 年 3 月 16 日,君实生物公告,其与旺山旺水公司合作开发的新冠药物 VV116 治疗中重度新冠患者的全球多中心 3 期临床试验,完成首例受试者给药。此外,VV116 治疗轻中度新冠患者的全球多中心 2/3 期临床试验也已经在中国完成首例给药。同日,该药在中国的 1 期临床数据在国际权威的 Nature 杂志发布。VV116 中国 1 期临床数据发布,新冠小分子快速推进中。①该药物在 86 名中国健康受试者中,展开了三项 I 期研究:研究 1(单次递增剂量研究)、研究 2(多次递增剂量研究)和研究 3(食物效应研究)。②受试者在口服 VV116 后,116-N1 的血浆药物峰值浓度迅速达到(中位 T?max?1.00-2.50 h);在 25-800 mg 的剂量范围内, AUC 和 C?max 以近似剂量比例的方式增加,而在 800 mg 的剂量下可能达到药物吸收饱和。受试者的标准膳食对 VV116 的 C?max和 AUC 没有影响;多次给药后,VV116 在 200 至 600 mg BID 剂量水平下达到了有效的抗病毒浓度。③研究结果显示,VV116 口服吸收迅速,重复给药可维持有效抗病毒浓度,普通饮食对药物暴露量无影响。
2022 年 3 月 16 日,君实生物公告,其与旺山旺水公司合作开发的新冠药物 VV116 治疗中重度新冠患者的全球多中心 3 期临床试验,完成首例受试者给药。此外,VV116 治疗轻中度新冠患者的全球多中心 2/3 期临床试验也已经在中国完成首例给药。同日,该药在中国的 1 期临床数据在国际权威的 Nature 杂志发布。VV116 中国 1 期临床数据发布,新冠小分子快速推进中。①该药物在 86 名中国健康受试者中,展开了三项 I 期研究:研究 1(单次递增剂量研究)、研究 2(多次递增剂量研究)和研究 3(食物效应研究)。②受试者在口服 VV116 后,116-N1 的血浆药物峰值浓度迅速达到(中位 T?max?1.00-2.50 h);在 25-800 mg 的剂量范围内, AUC 和 C?max 以近似剂量比例的方式增加,而在 800 mg 的剂量下可能达到药物吸收饱和。受试者的标准膳食对 VV116 的 C?max和 AUC 没有影响;多次给药后,VV116 在 200 至 600 mg BID 剂量水平下达到了有效的抗病毒浓度。③研究结果显示,VV116 口服吸收迅速,重复给药可维持有效抗病毒浓度,普通饮食对药物暴露量无影响。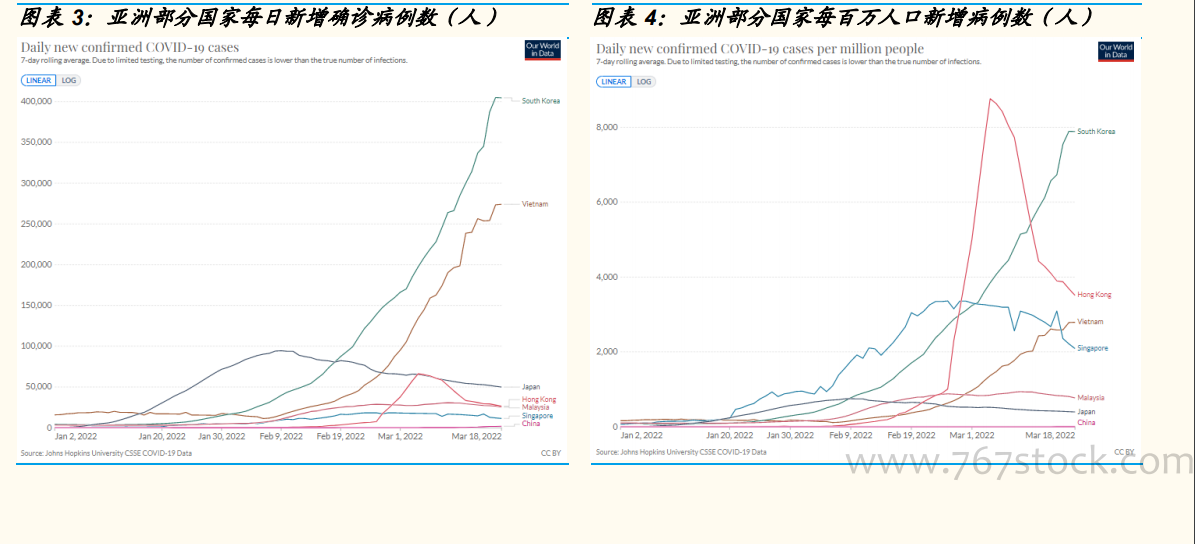
 3 月 15 日,国家卫健委发布《新型冠状病毒肺炎诊疗方案(试行第九版)》,新版诊疗方案针对德尔塔、奥密克戎等变异毒株传播特点和病理特征进行了修订。重点修订内容包括:①优化病例发现和报告程序。在核酸检测基础上,增加抗原检测作为补充,进一步提高病例早发现能力,同时提高疑似病例诊断或排除效率;②对病例实施分类收治,从之前的疑似及确诊病例全部在定点医院治疗,修改为轻型病例实行集中隔离管理、普通型/重型/危重型病例和有重型高危因素的病例应在定点医院集中治疗;③将国家药监局批准的两种特异性抗新冠病毒药物写入诊疗方案,即辉瑞新冠口服药Paxlovid(PF-07321332/利托那韦片)和腾盛博药中和抗体(安巴韦单抗/罗米司韦单抗注射液);④中医治疗内容进行了修订完善;⑤调整解除隔离管理、出院标准以及缩短了解除隔离管理、出院后监测时间。我们认为,新冠诊疗方案的调整一方面反映出我国在新冠检测、新冠特效药研发及批准、中医中药等特色医疗的应用等方面的阶段性成果,另一方面也适应了变异株带来的疫情特征的变化。
3 月 15 日,国家卫健委发布《新型冠状病毒肺炎诊疗方案(试行第九版)》,新版诊疗方案针对德尔塔、奥密克戎等变异毒株传播特点和病理特征进行了修订。重点修订内容包括:①优化病例发现和报告程序。在核酸检测基础上,增加抗原检测作为补充,进一步提高病例早发现能力,同时提高疑似病例诊断或排除效率;②对病例实施分类收治,从之前的疑似及确诊病例全部在定点医院治疗,修改为轻型病例实行集中隔离管理、普通型/重型/危重型病例和有重型高危因素的病例应在定点医院集中治疗;③将国家药监局批准的两种特异性抗新冠病毒药物写入诊疗方案,即辉瑞新冠口服药Paxlovid(PF-07321332/利托那韦片)和腾盛博药中和抗体(安巴韦单抗/罗米司韦单抗注射液);④中医治疗内容进行了修订完善;⑤调整解除隔离管理、出院标准以及缩短了解除隔离管理、出院后监测时间。我们认为,新冠诊疗方案的调整一方面反映出我国在新冠检测、新冠特效药研发及批准、中医中药等特色医疗的应用等方面的阶段性成果,另一方面也适应了变异株带来的疫情特征的变化。 2022 年 3 月 16 日,君实生物公告,其与旺山旺水公司合作开发的新冠药物 VV116 治疗中重度新冠患者的全球多中心 3 期临床试验,完成首例受试者给药。此外,VV116 治疗轻中度新冠患者的全球多中心 2/3 期临床试验也已经在中国完成首例给药。同日,该药在中国的 1 期临床数据在国际权威的 Nature 杂志发布。VV116 中国 1 期临床数据发布,新冠小分子快速推进中。①该药物在 86 名中国健康受试者中,展开了三项 I 期研究:研究 1(单次递增剂量研究)、研究 2(多次递增剂量研究)和研究 3(食物效应研究)。②受试者在口服 VV116 后,116-N1 的血浆药物峰值浓度迅速达到(中位 T?max?1.00-2.50 h);在 25-800 mg 的剂量范围内, AUC 和 C?max 以近似剂量比例的方式增加,而在 800 mg 的剂量下可能达到药物吸收饱和。受试者的标准膳食对 VV116 的 C?max和 AUC 没有影响;多次给药后,VV116 在 200 至 600 mg BID 剂量水平下达到了有效的抗病毒浓度。③研究结果显示,VV116 口服吸收迅速,重复给药可维持有效抗病毒浓度,普通饮食对药物暴露量无影响。
2022 年 3 月 16 日,君实生物公告,其与旺山旺水公司合作开发的新冠药物 VV116 治疗中重度新冠患者的全球多中心 3 期临床试验,完成首例受试者给药。此外,VV116 治疗轻中度新冠患者的全球多中心 2/3 期临床试验也已经在中国完成首例给药。同日,该药在中国的 1 期临床数据在国际权威的 Nature 杂志发布。VV116 中国 1 期临床数据发布,新冠小分子快速推进中。①该药物在 86 名中国健康受试者中,展开了三项 I 期研究:研究 1(单次递增剂量研究)、研究 2(多次递增剂量研究)和研究 3(食物效应研究)。②受试者在口服 VV116 后,116-N1 的血浆药物峰值浓度迅速达到(中位 T?max?1.00-2.50 h);在 25-800 mg 的剂量范围内, AUC 和 C?max 以近似剂量比例的方式增加,而在 800 mg 的剂量下可能达到药物吸收饱和。受试者的标准膳食对 VV116 的 C?max和 AUC 没有影响;多次给药后,VV116 在 200 至 600 mg BID 剂量水平下达到了有效的抗病毒浓度。③研究结果显示,VV116 口服吸收迅速,重复给药可维持有效抗病毒浓度,普通饮食对药物暴露量无影响。




