【行业】合成生物学-合聚万物,成致未来(51页)
合成生物学是指采用工程科学研究理念,对生物体进行有目标地设计、改造乃至重新合成,创建赋予非自然功能的“人造生命”,合成生物制造是以合成生物为工具进行物质加工与合成的生产方式,有望彻底变革未来医药、化工、食品、能源、材料、农业等传统行业。合成生物学内涵主要体现在两个方面:1)自上而下:目标导向的构建”人造生命” ,使用代谢和基因工程技术为活细胞赋予新功能,“人工基因组”是其核心内容,大片段基因组操作、改造以及大规模、高精度、低成本DNA合成是关键技术;2)自下而上:通过将“非生命”生物分子成分聚集在一起在体外创建新的生物系统,元件标准化→模块构建→底盘适配的线路以及对生命过程的途径、网络组成及其调控、设计与构建是核心内容,人工线路构建平台是其关键技术。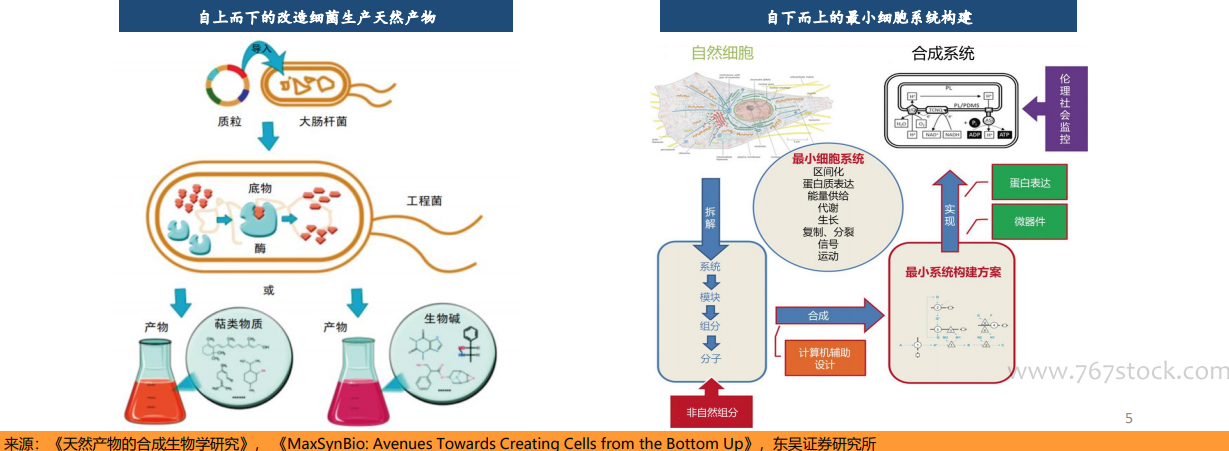 合成生物学的目的是设计符合标准的生物系统,基于工程设计原则利用工程可预测性控制复杂系统构建的“设计-构建-测试-学习”循环(DBTL)逐渐成为合成生物学的核心策略。生命系统具有高度的复杂性,人工设计的基因线路需要海量工程化试错实验去实现预设功能。这就需要用到“设计-构建-测试-学习”(DBTL)循环过程这一工程原理。在生物制造领域,DBLT循环四个阶段循环往复可以成功构建需要的细胞,生产出合适的产品。
合成生物学的目的是设计符合标准的生物系统,基于工程设计原则利用工程可预测性控制复杂系统构建的“设计-构建-测试-学习”循环(DBTL)逐渐成为合成生物学的核心策略。生命系统具有高度的复杂性,人工设计的基因线路需要海量工程化试错实验去实现预设功能。这就需要用到“设计-构建-测试-学习”(DBTL)循环过程这一工程原理。在生物制造领域,DBLT循环四个阶段循环往复可以成功构建需要的细胞,生产出合适的产品。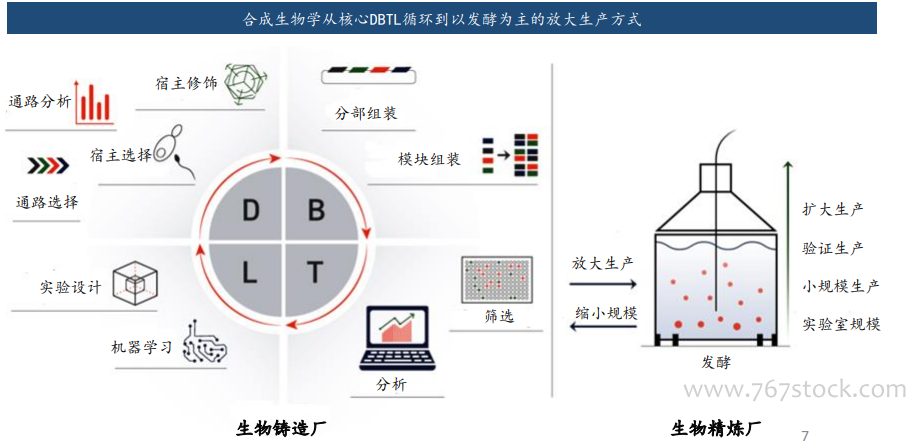 基因编辑技术的迭代:1996年,第一代代基因编辑技术,经基因工程改造的锌指核酸酶(ZFNs)被设计出来,开启人工改造生命体的旅程。2009年,第二代基因编辑技术类转录激活因子效应物核酸酶(TALENs)诞生。但前两代技术构建周期长,步骤繁琐,难以进行高通量基因编辑,极大限制了其推广应用。直到2012年,CRISPR技术横空出世,与ZFNs和TALENs技术相比, CRISPR/Cas9的设计要简单得多, 而且成本很低, 对于相同的靶点, CRISPR/Cas9有相当甚至更好的靶向效率。
基因编辑技术的迭代:1996年,第一代代基因编辑技术,经基因工程改造的锌指核酸酶(ZFNs)被设计出来,开启人工改造生命体的旅程。2009年,第二代基因编辑技术类转录激活因子效应物核酸酶(TALENs)诞生。但前两代技术构建周期长,步骤繁琐,难以进行高通量基因编辑,极大限制了其推广应用。直到2012年,CRISPR技术横空出世,与ZFNs和TALENs技术相比, CRISPR/Cas9的设计要简单得多, 而且成本很低, 对于相同的靶点, CRISPR/Cas9有相当甚至更好的靶向效率。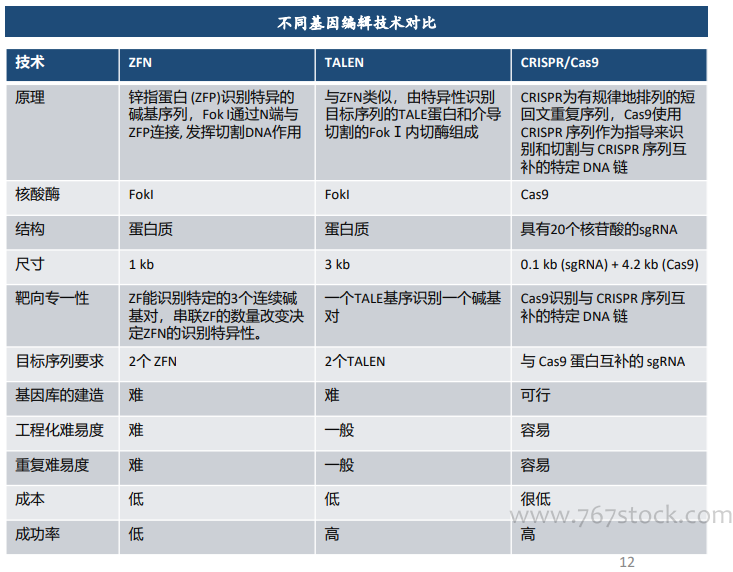
 合成生物学的目的是设计符合标准的生物系统,基于工程设计原则利用工程可预测性控制复杂系统构建的“设计-构建-测试-学习”循环(DBTL)逐渐成为合成生物学的核心策略。生命系统具有高度的复杂性,人工设计的基因线路需要海量工程化试错实验去实现预设功能。这就需要用到“设计-构建-测试-学习”(DBTL)循环过程这一工程原理。在生物制造领域,DBLT循环四个阶段循环往复可以成功构建需要的细胞,生产出合适的产品。
合成生物学的目的是设计符合标准的生物系统,基于工程设计原则利用工程可预测性控制复杂系统构建的“设计-构建-测试-学习”循环(DBTL)逐渐成为合成生物学的核心策略。生命系统具有高度的复杂性,人工设计的基因线路需要海量工程化试错实验去实现预设功能。这就需要用到“设计-构建-测试-学习”(DBTL)循环过程这一工程原理。在生物制造领域,DBLT循环四个阶段循环往复可以成功构建需要的细胞,生产出合适的产品。 基因编辑技术的迭代:1996年,第一代代基因编辑技术,经基因工程改造的锌指核酸酶(ZFNs)被设计出来,开启人工改造生命体的旅程。2009年,第二代基因编辑技术类转录激活因子效应物核酸酶(TALENs)诞生。但前两代技术构建周期长,步骤繁琐,难以进行高通量基因编辑,极大限制了其推广应用。直到2012年,CRISPR技术横空出世,与ZFNs和TALENs技术相比, CRISPR/Cas9的设计要简单得多, 而且成本很低, 对于相同的靶点, CRISPR/Cas9有相当甚至更好的靶向效率。
基因编辑技术的迭代:1996年,第一代代基因编辑技术,经基因工程改造的锌指核酸酶(ZFNs)被设计出来,开启人工改造生命体的旅程。2009年,第二代基因编辑技术类转录激活因子效应物核酸酶(TALENs)诞生。但前两代技术构建周期长,步骤繁琐,难以进行高通量基因编辑,极大限制了其推广应用。直到2012年,CRISPR技术横空出世,与ZFNs和TALENs技术相比, CRISPR/Cas9的设计要简单得多, 而且成本很低, 对于相同的靶点, CRISPR/Cas9有相当甚至更好的靶向效率。




