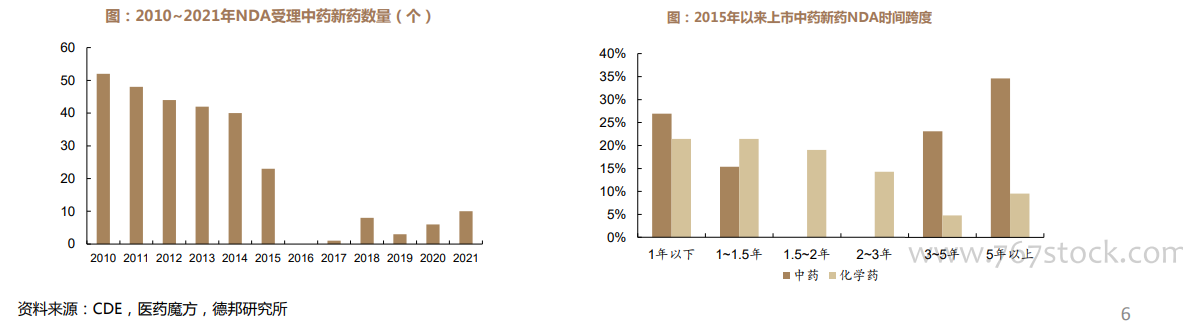【行业】中药-传承民族瑰宝,创新求实前行(44页)
国家层面政策导向延续,围绕“十四五”规划、健康中国顶层战略颁布全方位配套政策。22年3月国务院发布《“十四五”中医药发展规划》,中药顶层设计已初步完善。近期,二十大会议顶层设计再次明确要“促进中医药传承发展”,会中提及中药;十四五中医药人才规划出台,看好近期医保谈判及未来可能的基药目录调整机会。 近年中药注册管理制度持续优化,中药创新药概念得到明确界定。新版中药注册分类将“中药创新药”单独列出,进一步明确中药创新药概念,涵盖复方制剂、中药材及其制剂,新药材及其制剂。2022年11月药监局发布的《中药注册管理专门规定(征求意见稿)》中再次提出支持研制基于古代经典名方、名老中医方、医疗机构中药制剂等具有丰富中医临床实践经验的中药新药。
近年中药注册管理制度持续优化,中药创新药概念得到明确界定。新版中药注册分类将“中药创新药”单独列出,进一步明确中药创新药概念,涵盖复方制剂、中药材及其制剂,新药材及其制剂。2022年11月药监局发布的《中药注册管理专门规定(征求意见稿)》中再次提出支持研制基于古代经典名方、名老中医方、医疗机构中药制剂等具有丰富中医临床实践经验的中药新药。 平均来看中药新药研发跨度比化学药长,但近两年审评速度加快。中药新药NDA时间超过3年的数量占比为58%,化学药仅为14%。临床研发耗时较长的中药新药递交IND时间大都在2005年前,递交NDA时间大都在2010年前后,可能是由于申报过程中补充资料的要求延长了审评时间;但由于药品研发规范化、审评资料标准化以及审评中心效率的快速提升,NDA时间在2年以下的中药新药大都为近几年递交上市申请的品种,中药审评已有所加速。
平均来看中药新药研发跨度比化学药长,但近两年审评速度加快。中药新药NDA时间超过3年的数量占比为58%,化学药仅为14%。临床研发耗时较长的中药新药递交IND时间大都在2005年前,递交NDA时间大都在2010年前后,可能是由于申报过程中补充资料的要求延长了审评时间;但由于药品研发规范化、审评资料标准化以及审评中心效率的快速提升,NDA时间在2年以下的中药新药大都为近几年递交上市申请的品种,中药审评已有所加速。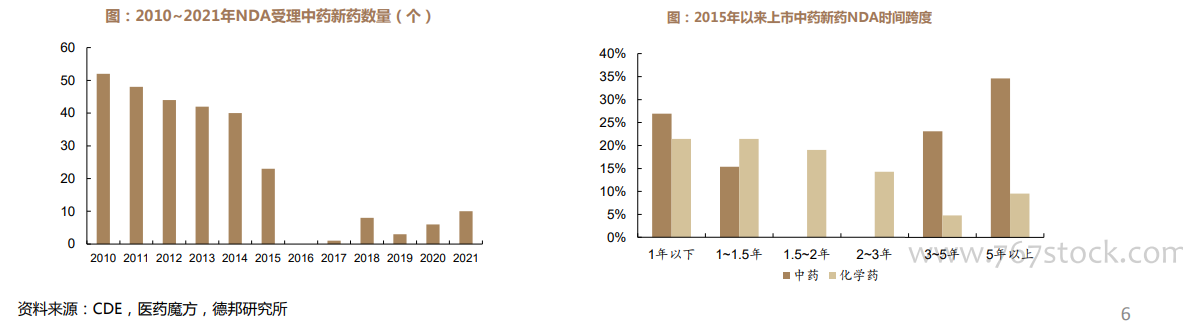
 近年中药注册管理制度持续优化,中药创新药概念得到明确界定。新版中药注册分类将“中药创新药”单独列出,进一步明确中药创新药概念,涵盖复方制剂、中药材及其制剂,新药材及其制剂。2022年11月药监局发布的《中药注册管理专门规定(征求意见稿)》中再次提出支持研制基于古代经典名方、名老中医方、医疗机构中药制剂等具有丰富中医临床实践经验的中药新药。
近年中药注册管理制度持续优化,中药创新药概念得到明确界定。新版中药注册分类将“中药创新药”单独列出,进一步明确中药创新药概念,涵盖复方制剂、中药材及其制剂,新药材及其制剂。2022年11月药监局发布的《中药注册管理专门规定(征求意见稿)》中再次提出支持研制基于古代经典名方、名老中医方、医疗机构中药制剂等具有丰富中医临床实践经验的中药新药。 平均来看中药新药研发跨度比化学药长,但近两年审评速度加快。中药新药NDA时间超过3年的数量占比为58%,化学药仅为14%。临床研发耗时较长的中药新药递交IND时间大都在2005年前,递交NDA时间大都在2010年前后,可能是由于申报过程中补充资料的要求延长了审评时间;但由于药品研发规范化、审评资料标准化以及审评中心效率的快速提升,NDA时间在2年以下的中药新药大都为近几年递交上市申请的品种,中药审评已有所加速。
平均来看中药新药研发跨度比化学药长,但近两年审评速度加快。中药新药NDA时间超过3年的数量占比为58%,化学药仅为14%。临床研发耗时较长的中药新药递交IND时间大都在2005年前,递交NDA时间大都在2010年前后,可能是由于申报过程中补充资料的要求延长了审评时间;但由于药品研发规范化、审评资料标准化以及审评中心效率的快速提升,NDA时间在2年以下的中药新药大都为近几年递交上市申请的品种,中药审评已有所加速。